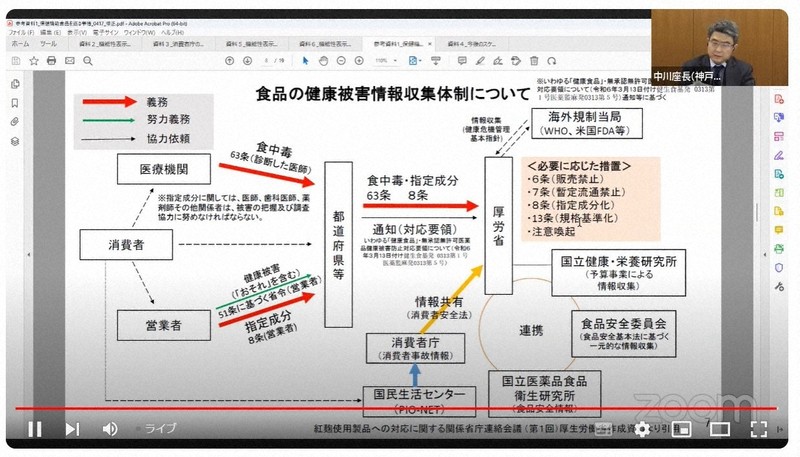
小林製薬(大阪市)の「紅こうじ」入りサプリメントの健康被害問題を受け、消費者庁は19日、サプリを届け出ていた機能性表示食品制度の見直しに向けた検討会の初会合を開いた。構成員の意見などから健康被害情報の報告ルールの整備などが焦点となりそうだ。
消費者事故調査安全委員会の委員長も務める中川丈久・神戸大教授が座長に選出された。制度導入時に検討会の委員だった合田幸広・国立医薬品食品衛生研究所名誉所長や神村裕子・日本医師会常任理事らも参加した。

機能性表示食品は、食品表示法に基づき2015年に導入された制度。事業者が食品の安全性と機能性に関する科学的根拠などを届け出れば健康効果を表示できる。合田氏は「機能性表示食品制度は事業者の性善説に基づいて作られた」と指摘。健康被害情報を把握した小林製薬の公表が2カ月ずれ込んだ点を鑑みて「食品でトラブルが起きた時に情報提供があまりにも遅く、国に届け出ないことも多い」と報告体制の不備に言及した。
品質管理体制の確保についても意見が相次いだ。機能性表示食品制度のガイドラインでは「適正な品質管理の規範(GMP)」の認証を推奨していたが、小林製薬の大阪工場は取得しておらず、神村氏は「GMPにきちんと入っていれば途中で成分がおかしいということは把握できたはずだ」との私見を述べた。
消費者庁は検討会の意見を踏まえ、5月末をめどに見直し案をまとめる。
厚生労働省も食品の安全確保を定める食品衛生法の観点から新たなルール作りを検討する。武見敬三厚労相は3日の衆院厚労委員会で「新たなルール化が必要だ。食品衛生法において、いかなる施策が必要か検討したい」と述べている。
焦点になるのは、サプリの位置づけだ。医薬品では、重大な副作用を製薬企業が把握した場合、国への報告が医薬品医療機器法で義務付けられているが、食品全般を対象とする食品衛生法に義務規定はない。
与党幹部は「新たに健康食品といった枠組みを作ることが考えられる」と指摘。被害発生時の報告義務や服用に関する制限なども焦点となりそうだが、法的な規制となれば見直しに時間がかかる可能性がある。【阿部絢美、肥沼直寛、宇多川はるか】
鄭重声明:本文の著作権は原作者に帰属します。記事の転載は情報の伝達のみを目的としており、投資の助言を構成するものではありません。もし侵害行為があれば、すぐにご連絡ください。修正または削除いたします。ありがとうございます。